Nota Sains Bab 6 Tingkatan 5: ELEKTROKIMIA
Sains Tingkatan 5
Bab 6: Elektrokimia
Sel Elektrolitik & Sel Kimia
Terminologi Elektrokimia
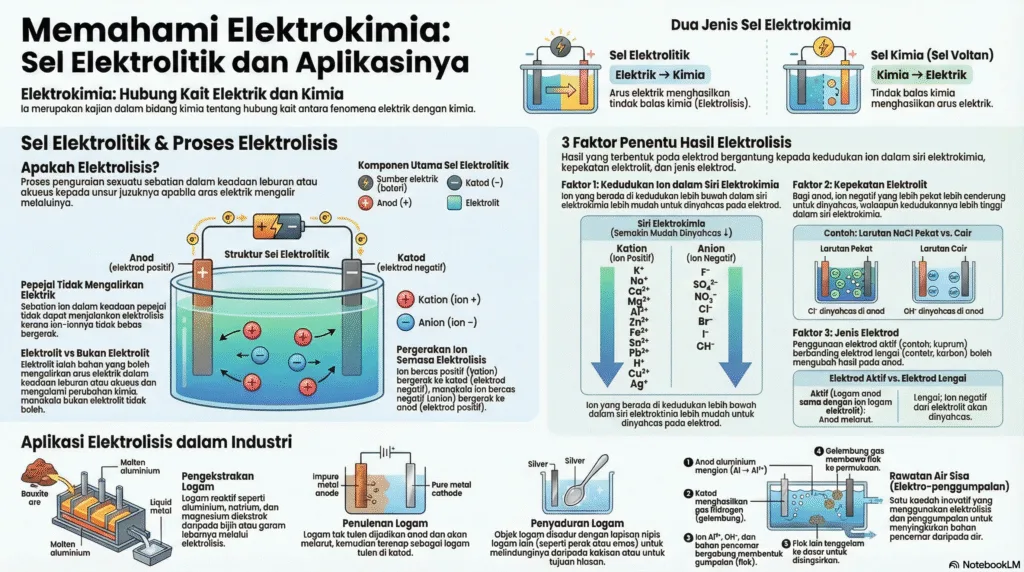
Elektrokimia ialah kajian tentang hubung kait antara tenaga elektrik dan tenaga kimia.
Elektrolit
Bahan Konduktor
Bahan yang dapat mengalirkan arus elektrik dalam keadaan leburan atau larutan akueus kerana mempunyai ion-ion yang bebas bergerak.
Anod (+)
Elektrod Positif
Elektrod yang disambungkan pada terminal positif sumber elektrik. Tempat di mana proses pengoksidaan berlaku.
Katod (-)
Elektrod Negatif
Elektrod yang disambungkan pada terminal negatif sumber elektrik. Tempat di mana proses penurunan berlaku.
Anion
Ion Negatif
Zarah yang bercas negatif. Ia akan tertarik dan bergerak menuju ke arah Anod (+) semasa proses elektrolisis.
Kation
Ion Positif
Zarah yang bercas positif. Ia akan tertarik dan bergerak menuju ke arah Katod (-) semasa proses elektrolisis.
Elektrod
Konduktor Elektrik
Bahan konduktor (seperti Karbon/Grafit atau Logam Kuprum) yang direndam dalam elektrolit untuk mengalirkan arus elektrik dari litar luar.
Simulator Sel Elektrolitik
Proses Elektrolisis: Tenaga Elektrik $\rightarrow$ Tenaga Kimia. Hidupkan suis untuk melihat pergerakan ion.
Pemerhatian Elektrolisis
Suis dimatikan. Ion-ion (Kation dan Anion) bergerak bebas secara rawak di dalam elektrolit.
Di Anod (+)
Ion negatif (Anion: Cl⁻, OH⁻) ditarik ke Anod. Ion Cl⁻ dinyahcas melepaskan elektron membentuk Gas Klorin (gelembung kuning kehijauan).
Di Katod (-)
Ion positif (Kation: Na⁺, H⁺) ditarik ke Katod. Ion H⁺ dinyahcas menerima elektron membentuk Gas Hidrogen (gelembung tidak berwarna).
3 Faktor Pemilihan Ion Untuk Dinyahcas
Aplikasi Elektrolisis Dalam Industri
Elektrolisis mempunyai banyak kegunaan praktikal dalam pelbagai sektor industri.
Pengekstrakan Logam
Mengekstrak logam yang sangat reaktif (seperti Aluminium, Magnesium, Natrium) daripada bijihnya.
Bijih bauksit (Aluminium oksida lebur) dileburkan. Ion Aluminium (Al³⁺) ditarik ke Katod lalu membentuk logam aluminium tulen.
Penulenan Logam
Menulenkan logam yang mempunyai bendasing kepada tahap ketulenan 99.9% (seperti Kuprum untuk wayar elektrik).
• Anod (+): Logam Tidak Tulen (Akan melarut)
• Katod (-): Logam Tulen (Menjadi tebal)
• Elektrolit: Larutan garam logam tersebut.
Penyaduran Logam
Menyalut suatu permukaan logam dengan lapisan nipis logam lain untuk menjadikannya lebih cantik dan mencegah kakisan (karat).
• Anod (+): Kepingan Emas tulen
• Katod (-): Objek yang disadur (Cincin besi)
• Elektrolit: Larutan Kuprum/Emas.
Pengolahan Air Sisa
Menggunakan teknik Elektro-penggumpalan untuk merawat air sisa kilang agar selamat dibuang ke sungai.
Elektrod Aluminium/Besi digunakan. Di Anod, ion Al³⁺ terhasil dan menggumpalkan (coagulate) bahan pencemar menjadi gumpalan besar (flok) yang boleh ditapis. Gelembung gas di Katod pula menolak flok terapung ke atas (flotasi).
Makmal Maya: Sel Kimia Ringkas (Bateri Buah)
Proses Sel Kimia/Voltan: Tenaga Kimia $\rightarrow$ Tenaga Elektrik. Pilih pasangan logam untuk melihat bacaan Voltan.
Pilihan Elektrod
Ditetapkan sebagai rujukan
Prinsip Sel Kimia (Prinsip Beza Keupayaan)
Logam yang berada di kedudukan yang lebih tinggi dalam Siri Elektrokimia (lebih reaktif) bertindak sebagai Terminal Negatif (menderma elektron).
Semakin jauh kedudukan antara dua logam tersebut di dalam Siri Elektrokimia, semakin besar nilai voltan (tenaga elektrik) yang dihasilkan.
Elektrokimia
Sains Tingkatan 5 (Bab 6)
Ujian interaktif ini memuatkan 10 Soalan Rawak yang akan mencabar kefahaman anda tentang sel elektrolitik, sel kimia, pengekstrakan logam, penyaduran, dan siri elektrokimia.
“Aliran cas menghasilkan tenaga, adakah litar minda anda sudah bersedia?”
Menyambungkan arus…
Ujian Selesai
Laporan Voltan Kognitif Anda:
Keterangan log maklum balas sains di sini.
KOLEKSI LATIHAN
KOLEKSI LATIHAN
| LATIHAN | SKEMA JAWAPAN |
|---|---|
GLOSARI
Terma & Definisi Elektrokimia
GLOSARI
Terma & Definisi Elektrokimia
Ion yang bercas negatif yang bergerak ke anod semasa elektrolisis.
Elektrod positif dalam sel elektrolitik yang menarik anion.
Proses penguraian sebatian kimia menggunakan arus elektrik.
Bahan yang mengalirkan elektrik dalam keadaan leburan atau akueus.
Ion bercas positif yang bergerak ke arah katod semasa elektrolisis.
Elektrod negatif dalam sel elektrolitik yang menarik kation.
Sel yang menukarkan tenaga kimia kepada tenaga elektrik secara spontan.
Susunan ion mengikut kecenderungan untuk dinyahcas pada elektrod.
⚡
CONTOH SOALAN KBAT
Elektrokimia (Kemahiran Berfikir Aras Tinggi)
CONTOH SOALAN KBAT
Elektrokimia (Kemahiran Berfikir Aras Tinggi)
- Katod: Enapan Perak (Ag) terbentuk karena Ag⁺ lebih mudah dinyahcas daripada H⁺.
- Anod: Gas Oksigen terbebas karena OH⁻ lebih mudah dinyahcas daripada NO₃⁻.
🚀
Zon Interaktif
⚡
Jana tenaga ilmu dengan aktiviti interaktif!
Zon Interaktif
⚡Jana tenaga ilmu dengan aktiviti interaktif!
