Nota Sains Bab 6 Tingkatan 5: ELEKTROKIMIA
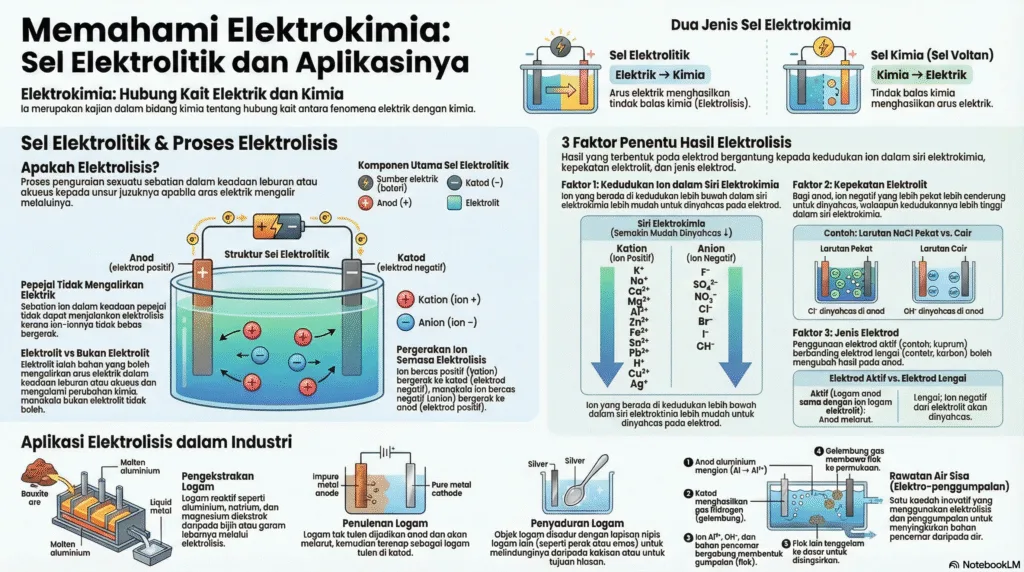
Elektrokimia
Ketahui rahsia penukaran tenaga elektrik kepada kimia dan sebaliknya! Fahami konsep sel elektrolitik, sel kimia, serta peranan siri elektrokimia dalam kehidupan.
Apakah itu Elektrolisis?
Elektrolisis ialah proses penguraian suatu sebatian kimia (elektrolit) dalam keadaan leburan atau akueus kepada unsur juzuknya apabila arus elektrik dialirkan melaluinya.
Simulasi: Migrasi & Nyahcas Ion
Pilih jenis elektrolit di bawah dan klik “Mula Aliran Elektrik” untuk melihat bagaimana ion-ion bergerak ke elektrod masing-masing!
🧪 Pilih Elektrolit Akueus:
1. **Kedudukan dalam Siri Elektrokimia**: Ion di kedudukan lebih rendah lebih mudah dinyahcas (Contoh: $\text{Cu}^{2+}$ berbanding $\text{H}^+$).
2. **Kepekatan**: Ion yang lebih pekat di dalam larutan akan dipilih untuk dinyahcas di Anod (Contoh: $\text{Cl}^-$ dinyahcas menghasilkan gas klorina).
👀 Beaker Sel Elektrolitik Pasif:
Tips Mengingat Cepat untuk SPM
Ingat akronim migrasi: **Kation** (ion positif) bergerak ke **Katod** (terminal negatif)! Manakala **Anion** (ion negatif) bergerak ke **Anod** (terminal positif) semasa proses elektrolisis!
Lubuk Pembelajaran Terbaik & Koleksi Soalan SPM Terkini
KOLEKSI LATIHAN
KOLEKSI LATIHAN
| LATIHAN | SKEMA JAWAPAN |
|---|---|
GLOSARI
Terma & Definisi Elektrokimia
GLOSARI
Terma & Definisi Elektrokimia
Ion yang bercas negatif yang bergerak ke anod semasa elektrolisis.
Elektrod positif dalam sel elektrolitik yang menarik anion.
Proses penguraian sebatian kimia menggunakan arus elektrik.
Bahan yang mengalirkan elektrik dalam keadaan leburan atau akueus.
Ion bercas positif yang bergerak ke arah katod semasa elektrolisis.
Elektrod negatif dalam sel elektrolitik yang menarik kation.
Sel yang menukarkan tenaga kimia kepada tenaga elektrik secara spontan.
Susunan ion mengikut kecenderungan untuk dinyahcas pada elektrod.
⚡CONTOH SOALAN KBAT
Elektrokimia (Kemahiran Berfikir Aras Tinggi)
CONTOH SOALAN KBAT
Elektrokimia (Kemahiran Berfikir Aras Tinggi)
- Katod: Enapan Perak (Ag) terbentuk karena Ag⁺ lebih mudah dinyahcas daripada H⁺.
- Anod: Gas Oksigen terbebas karena OH⁻ lebih mudah dinyahcas daripada NO₃⁻.
🚀Zon Interaktif
⚡Jana tenaga ilmu dengan aktiviti interaktif!
Zon Interaktif
⚡Jana tenaga ilmu dengan aktiviti interaktif!
