Nota Sains Tambahan Tingkatan 4 Bab 4: Stoikiometri
Sains Tambahan: Tingkatan 4
BAB 4: Stoikiometri
⚗️4.1 Jisim Atom, Molekul & Formula Relatif
Atom adalah terlalu kecil untuk ditimbang satu per satu. Oleh itu, jisimnya dibandingkan dengan satu atom piawai iaitu Karbon-12.
Jisim Atom Relatif (JAR)
Jisim purata satu atom unsur berbanding dengan 1/12 daripada jisim satu atom karbon-12.
Jisim Molekul Relatif (JMR)
Sama seperti JAR tetapi untuk molekul kovalen. Ia adalah hasil tambah JAR bagi semua atom dalam molekul tersebut.
Jisim Formula Relatif (JFR)
Hasil tambah JAR bagi semua atom dalam sebatian ionik (kerana sebatian ion tidak wujud sebagai molekul diskret).
Contoh Pengiraan JMR
4.2 Konsep Mol & Pemalar Avogadro
Satu mol bahan mengandungi bilangan zarah yang sama dengan bilangan atom karbon di dalam 12 gram Karbon-12.
Pemalar Avogadro (NA)
1 mol apa jua bahan akan mengandungi 6.02 × 1023 zarah (atom / molekul / ion).
Penukaran Unit Mol (Segi Tiga Hubungan)
Jisim (g)
(Sama nilai dgn JAR/JMR)
MOL
Bilangan Zarah
(6.02 × 1023)
4.3 Formula Kimia
Perwakilan suatu bahan kimia dengan menggunakan huruf mewakili atom dan nombor subskrip mewakili bilangannya.
🔋 Pembentukan Ion
Kation (+) ➕
Terbentuk apabila atom logam menderma elektron. Bilangan proton melebihi elektron.
Cth: Na → Na+ + e–
Anion (-) ➖
Terbentuk apabila atom bukan logam menerima elektron. Bilangan elektron melebihi proton.
Cth: Cl + e– → Cl–
✖️ Kaedah Silang Cas
Untuk menulis formula sebatian ion, nilai cas (tanpa tanda + atau -) disilangkan untuk menjadi nombor subskrip.
*Jika cas sama (contoh Mg2+ & O2-), nombor diringkaskan menjadi MgO.
4.4 Persamaan Kimia & Stoikiometri
Persamaan kimia menceritakan tindak balas secara kuantitatif. Ia mesti seimbang bagi mematuhi Hukum Keabadian Jisim.
Mentafsir Persamaan Kimia
Kiri anak panah (N2 & H2)
Nombor besar di depan menunjukkan Nisbah Mol.
Kanan anak panah (NH3)
Maksud: “1 mol gas Nitrogen bertindak balas dengan 3 mol gas Hidrogen untuk menghasilkan 2 mol gas Ammonia.”
3 Langkah Menyelesaikan Masalah Stoikiometri
Cari Mol Maklumat Beri
Tukar jisim / isipadu / bilangan zarah yang diberikan dalam soalan kepada unit mol.
Nisbah Mol
Gunakan persamaan kimia seimbang untuk mencari nisbah mol bahan yang dicari.
Cari Jawapan Akhir
Tukar unit mol bahan yang dicari kepada jisim / isipadu / bilangan zarah yang dikehendaki soalan.
Sains Tambahan Tingkatan 4 © Modul Kimia Digital
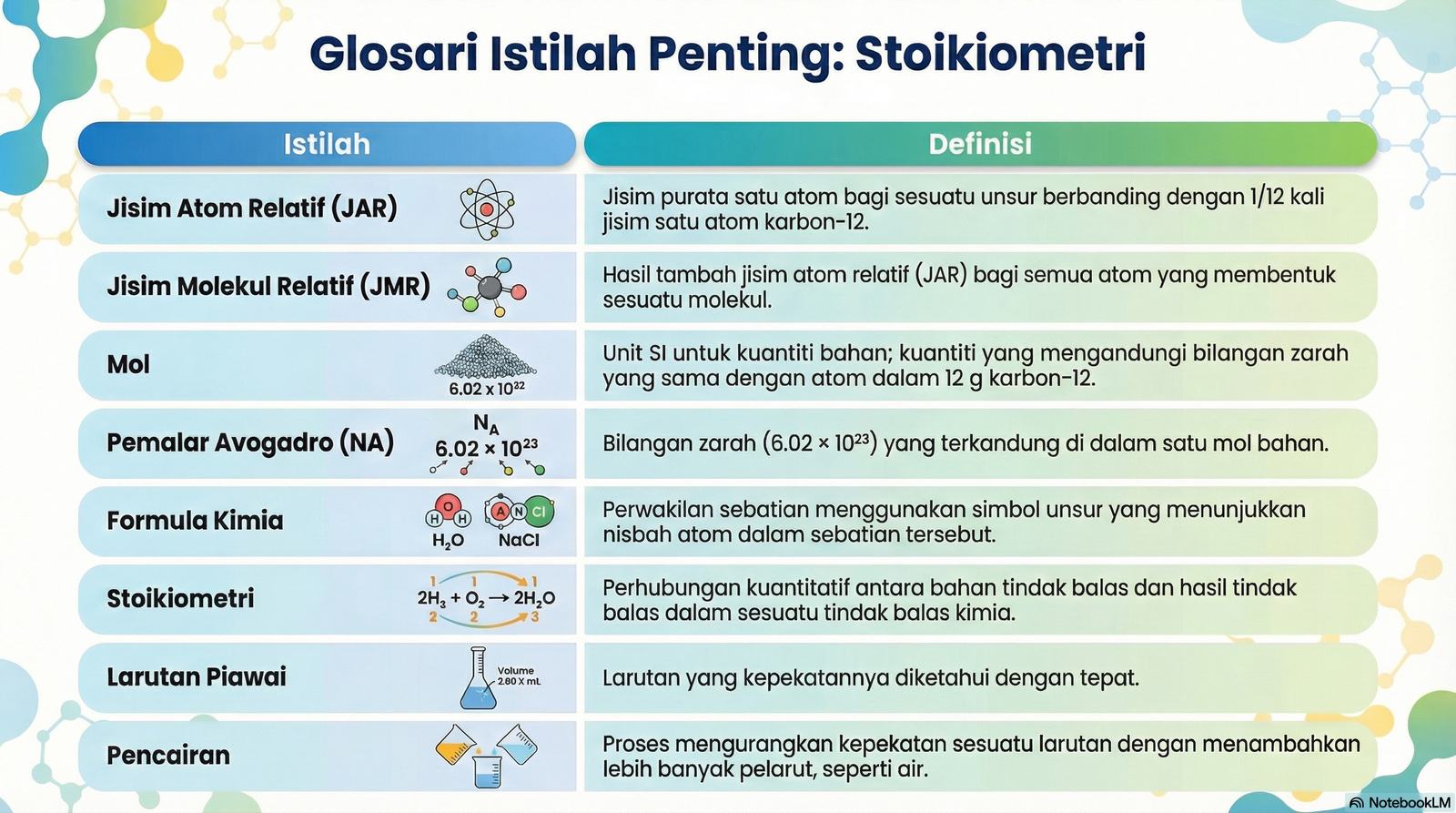
GLOSARI: FORMULA & PERSAMAAN KIMIA
| Istilah | Definisi |
|---|---|
| Atom | Zarah terkecil bagi sesuatu unsur. |
| Duplet | Susunan elektron yang stabil dengan dua elektron di petala terluar. |
| Formula Kimia | Perwakilan sebatian menggunakan simbol unsur dan subskrip nombor untuk menunjukkan jenis dan bilangan atom. |
| Ion | Zarah bercas yang terbentuk apabila suatu atom menderma atau menerima elektron. |
| Anion & Kation | Anion: Ion negatif (terima elektron). Kation: Ion positif (derma elektron). |
| JAR / JMR / JFR | Jisim Relatif atom (JAR), molekul (JMR), atau formula (JFR) berbanding 1/12 jisim satu atom karbon-12. |
| Jisim Molar | Jisim bagi satu mol sesuatu bahan (g mol⁻¹). |
| Kemolaran (M) | Unit kepekatan (bilangan mol zat terlarut per dm³ larutan). |
| Larutan Piawai | Larutan yang kepekatannya diketahui dengan tepat. |
| Mol | Unit SI kuantiti bahan. Satu mol mengandungi 6.02 × 10²³ zarah. |
| Oktet | Susunan elektron stabil dengan lapan elektron di petala terluar. |
| Pekali | Angka di hadapan formula kimia untuk menyeimbangkan persamaan kimia. |
| Pencairan | Proses mengurangkan kepekatan larutan dengan menambah pelarut. |
| Persamaan Kimia | Perwakilan tindak balas kimia menggunakan formula kimia (Bahan → Hasil). |
| Stoikiometri | Kajian hubungan kuantitatif antara bahan dan hasil dalam tindak balas kimia. |
| Zarah | Istilah umum merujuk kepada atom, molekul atau ion. |
