Nota Sains Tambahan Tingkatan 4 Bab 5: Ikatan Kimia
Sains Tambahan: Tingkatan 4
BAB 5: Ikatan Kimia
⚛️5.1 Kestabilan Unsur & Gas Adi
Unsur-unsur bergabung membentuk ikatan kimia untuk mencapai susunan elektron yang stabil seperti Gas Adi (Kumpulan 18).
Susunan Duplet
Mempunyai maksimum 2 elektron valens pada petala pertama (dan satu-satunya petala).
Susunan elektron: 2
Susunan Oktet
Mempunyai maksimum 8 elektron valens pada petala paling luar.
Susunan elektron Ne: 2.8
Bagaimana Unsur Lain Mencapai Kestabilan?
Menderma Elektron
Berlaku pada atom Logam (Kump 1, 2, 13) yang mempunyai 1, 2, atau 3 elektron valens.
Menerima Elektron
Berlaku pada atom Bukan Logam (Kump 15, 16, 17) yang mempunyai 5, 6, atau 7 elektron valens.
Berkongsi Elektron
Berlaku antara atom Bukan Logam dengan Bukan Logam yang masing-masing memerlukan elektron.
5.2 Ikatan Ion (Ikatan Elektrovalen)
Ikatan yang terbentuk akibat daripada pemindahan elektron daripada atom logam kepada atom bukan logam.
🧲 Proses Pembentukan Ikatan Ion
Atom Logam
Cth: Natrium (Na) 2.8.1
Ion Positif (Kation)
Atom Bukan Logam
Cth: Klorin (Cl) 2.8.7
Ion Negatif (Anion)
Ion Na+ dan ion Cl– yang berlainan cas akan ditarik oleh Daya Tarikan Elektrostatik yang kuat untuk membentuk sebatian ion Natrium Klorida (NaCl).
Sifat Fizik Sebatian Ion
Takat Lebur & Didih TINGGI
Daya tarikan elektrostatik antara ion adalah sangat kuat. Banyak tenaga haba diperlukan untuk memutuskannya.
Mengkonduksi Elektrik
Boleh mengkonduksi elektrik dalam keadaan leburan atau akueus (kerana ion bebas bergerak). Tidak boleh dalam keadaan pepejal.
Keterlarutan
Biasanya larut dalam air (pelarut inorganik), tetapi tidak larut dalam pelarut organik (seperti eter/aseton).
5.3 Ikatan Kovalen
Ikatan yang terbentuk apabila atom-atom bukan logam berkongsi elektron sesama sendiri untuk mencapai susunan elektron duplet atau oktet yang stabil.
Berkongsi 1 pasang elektron (2 elektron).
Berkongsi 2 pasang elektron (4 elektron).
Sifat Fizik Sebatian Kovalen
Takat Lebur & Didih RENDAH
Molekul ditarik oleh daya tarikan Van der Waals yang sangat lemah. Sedikit haba diperlukan untuk memisahkannya. (Wujud sbg gas/cecair pd suhu bilik).
Tidak Mengkonduksi Elektrik
Tidak mempunyai ion-ion yang bergerak bebas dalam sebarang keadaan (pepejal/cecair/gas).
Keterlarutan
Biasanya tidak larut dalam air, tetapi sangat larut dalam pelarut organik (seperti kloroform, aseton, alkohol).
Aplikasi Sebatian Kovalen dalam Kehidupan
Kebanyakan bahan organik adalah sebatian kovalen. Contohnya bahan pencuci, kosmetik, cat, ubat-ubatan, plastik, dan juga air (H2O) serta karbon dioksida (CO2).
Sains Tambahan Tingkatan 4 © Modul Ikatan Kimia Digital
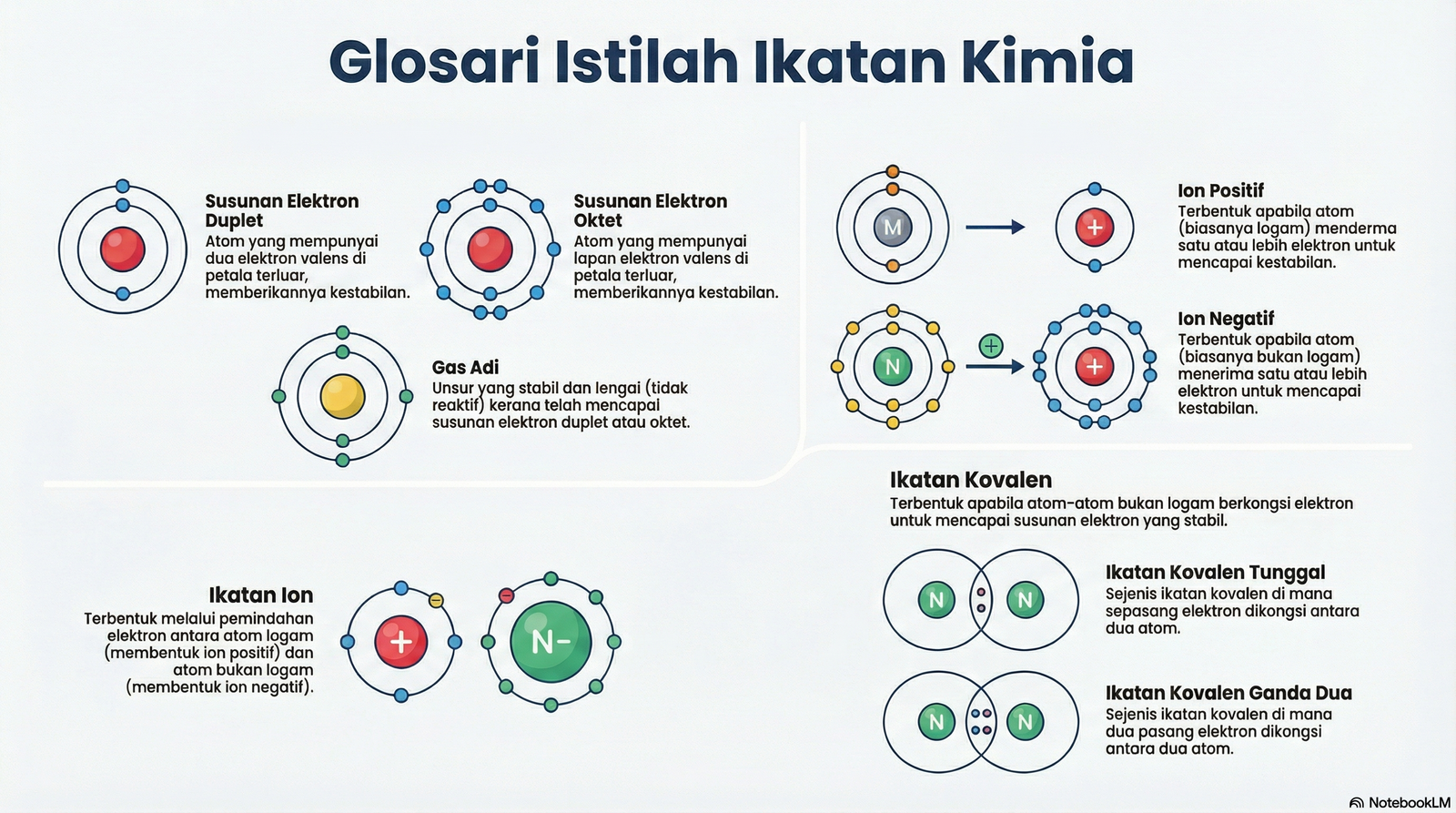
GLOSARI: IKATAN KIMIA
| Istilah | Definisi |
|---|---|
| Duplet | Susunan elektron yang stabil di mana petala elektron terluar atom diisi dengan dua elektron. |
| Elektron valens | Elektron yang terletak di petala paling luar bagi sesuatu atom. |
| Gas adi | Unsur-unsur Kumpulan 18 yang stabil secara kimia karena mempunyai susunan elektron duplet atau oktet yang penuh. |
| Ikatan Ion | Ikatan hasil daya tarikan elektrostatik antara ion bercas positif (kation) dan negatif (anion) selepas pemindahan elektron. |
| Ikatan Kovalen | Ikatan yang terbentuk apabila atom-atom bukan logam berkongsi pasangan elektron untuk mencapai susunan stabil. |
| Kovalen Ganda Dua | Ikatan kovalen yang terbentuk apabila dua atom berkongsi dua pasang elektron (empat elektron). |
| Kovalen Tunggal | Ikatan kovalen yang terbentuk apabila dua atom berkongsi sepasang elektron (dua elektron). |
| Anion | Ion negatif yang terbentuk apabila atom atau kumpulan atom menerima satu atau lebih elektron. |
| Kation | Ion positif yang terbentuk apabila atom atau kumpulan atom menderma satu atau lebih elektron. |
| Lengai | Sifat suatu bahan kimia yang tidak reaktif atau tidak mudah bertindak balas dengan bahan lain. |
| Monoatom | Terdiri daripada satu atom sahaja dan tidak terikat secara kimia dengan atom lain. |
| Oktet | Susunan elektron yang stabil di mana petala elektron terluar atom diisi dengan lapan elektron. |
| Susunan elektron | Taburan atau kedudukan elektron dalam petala-petala yang mengelilingi nukleus sesuatu atom. |
