Nota Sains Tambahan Tingkatan 4 Bab 6: Tenaga dan Perubahan Kimia
Sains Tambahan: Tingkatan 4
BAB 6: Tenaga dan Perubahan Kimia
🔋Asas Pengoksidaan dan Penurunan
Satu proses penting dalam elektrokimia yang difokuskan kepada pemindahan elektron (e⁻) di antara bahan tindak balas.
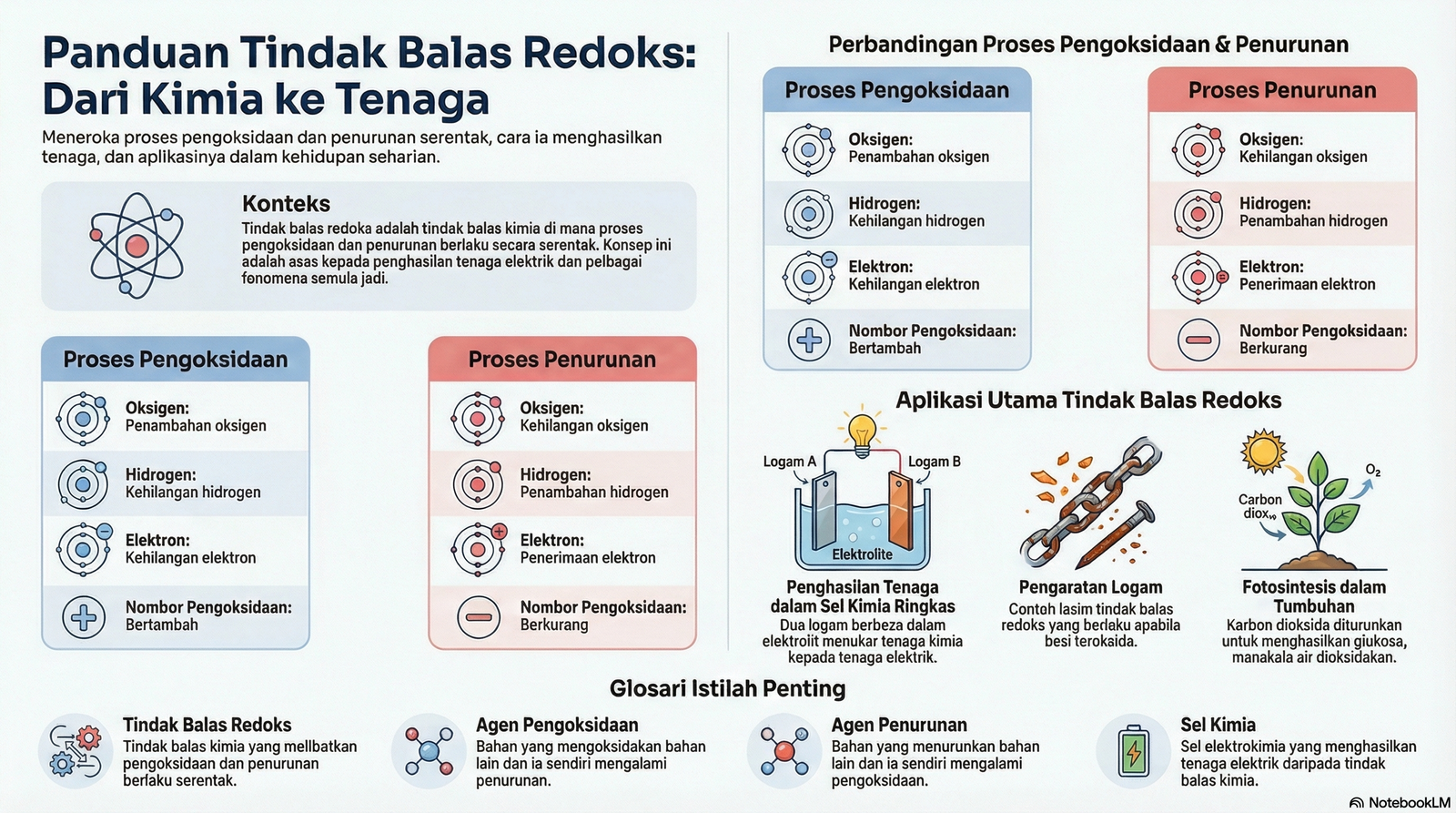
📤 Pengoksidaan
Proses PENYINGKIRAN (menderma) elektron.
Apabila satu atom/ion menderma elektron, nombor pengoksidaannya akan bertambah (menjadi lebih positif).
Mg → Mg2+ + 2e⁻
📥 Penurunan
Proses PENERIMAAN (menambah) elektron.
Apabila satu atom/ion menerima elektron, nombor pengoksidaannya akan berkurang (menjadi lebih negatif).
Cu2+ + 2e⁻ → Cu
Petua Mengingat (Mnemonic)
Penghasilan Tenaga Elektrik
Tenaga elektrik boleh dijanakan daripada tindak balas kimia melalui alat yang dipanggil Sel Kimia Ringkas (Sel Voltan).
Struktur Sel Kimia Ringkas
Terminal Negatif (Anod)
Logam yang lebih reaktif (kedudukan tinggi dlm Siri Elektrokimia).
- Melepaskan elektron.
- Mengalami proses Pengoksidaan.
- Elektrod semakin menipis.
Terminal Positif (Katod)
Logam yang kurang reaktif.
- Menerima elektron dari litar luar.
- Mengalami proses Penurunan.
- Elektrod menebal (pepejal terenap).
6.2 Tindak Balas Redoks
Singkatan bagi REDuction (Penurunan) dan OXidation (Pengoksidaan). Tindak balas di mana kedua-dua proses ini berlaku secara serentak.
🧪 Tindak Balas Sesaran Logam (Contoh Redoks)
Apabila pita Magnesium dimasukkan ke dalam larutan Kuprum(II) sulfat yang berwarna biru:
Proses Pengoksidaan
Atom Magnesium melepaskan elektron membentuk ion Magnesium.
→ Mg bertindak sebagai Agen Penurunan
Proses Penurunan
Ion Kuprum(II) dalam larutan menerima elektron membentuk atom Kuprum.
→ Ion Cu2+ bertindak sebagai Agen Pengoksidaan
Pemerhatian Ekperimen:
- Pita magnesium melarut / menipis.
- Pepejal perang (Kuprum) dienapkan.
- Warna biru larutan Kuprum(II) sulfat pudar menjadi tidak berwarna (MgSO4).
Aplikasi Redoks dalam Kehidupan
Bateri (Sel Kering)
Menjana arus elektrik mudah alih. Menggunakan zink sebagai anod dan grafit sebagai katod dalam tindak balas redoks terkawal.
Pengaratan Besi
Tindak balas redoks semula jadi. Besi teroksida apabila terdedah kepada oksigen dan air membentuk ferum(III) oksida terhidrat (karat).
Pengekstrakan Logam
Proses penurunan bijih logam (seperti timah / besi) menggunakan karbon untuk memisahkan logam tulen dari oksigennya.
Sains Tambahan Tingkatan 4 © Modul Elektrokimia Digital
GLOSARI: TINDAK BALAS KIMIA
| Istilah | Definisi |
|---|---|
| Agen Pengoksidaan | Bahan yang mengoksidakan bahan lain dan ia sendiri diturunkan dalam tindak balas kimia. |
| Agen Penurunan | Bahan yang menurunkan bahan lain dan ia sendiri dioksidakan dalam tindak balas kimia. |
| Anod | Terminal negatif dalam sel kimia, di mana proses pengoksidaan (kehilangan elektron) berlaku. |
| Elektrod | Logam-logam yang disambung dengan wayar penyambung dalam sebuah sel kimia untuk mengalirkan arus. |
| Elektrolit | Larutan yang membenarkan pengaliran ion, melengkapkan litar dalam sel kimia. |
| Katod | Terminal positif dalam sel kimia, di mana proses penurunan (penerimaan elektron) berlaku. |
| Pengoksidaan | Proses penambahan oksigen, kehilangan hidrogen, kehilangan elektron, atau pertambahan nombor pengoksidaan. |
| Penurunan | Proses kehilangan oksigen, penambahan hidrogen, penerimaan elektron, atau pengurangan nombor pengoksidaan. |
| Sel Kimia Ringkas | Sel yang menghasilkan tenaga elektrik daripada tindak balas kimia menggunakan dua logam berbeza. |
| Siri Elektrokimia | Susunan logam mengikut kecenderungan menderma elektron. Logam di atas lebih mudah menderma elektron. |
| Tindak Balas Redoks | Tindak balas kimia di mana proses pengoksidaan dan penurunan berlaku secara serentak. |
| Pengaratan | Satu contoh tindak balas redoks yang melibatkan pengoksidaan besi oleh oksigen dan air. |
