Glosari SPM Kimia – Tingkatan 4 bab 4
Glosari Kimia Digital
Bab 3: Konsep Mol & Bab 4: Jadual Berkala
Formula Empirik
Formula yang menunjukkan nisbah paling ringkas bilangan atom setiap unsur dalam sebatian.
Bab 3Isi Padu Molar
Isi padu bagi 1 mol sebarang gas pada suhu dan tekanan tertentu.
Jisim Molar
Jisim bagi satu mol sesuatu bahan. Sama dengan JAR/JMR dalam gram.
Mol
Unit kuantiti bahan yang mengandungi bilangan zarah bersamaan dengan 6.02 × 1023.
Bab 3Pemalar Avogadro
Bilangan zarah (atom, molekul atau ion) dalam satu mol bahan.
STP
Suhu dan Tekanan Piawai: Suhu 0°C dan tekanan 1 atm.
Bab 3Elektron Valens
Elektron yang berada di petala paling luar sesuatu atom.
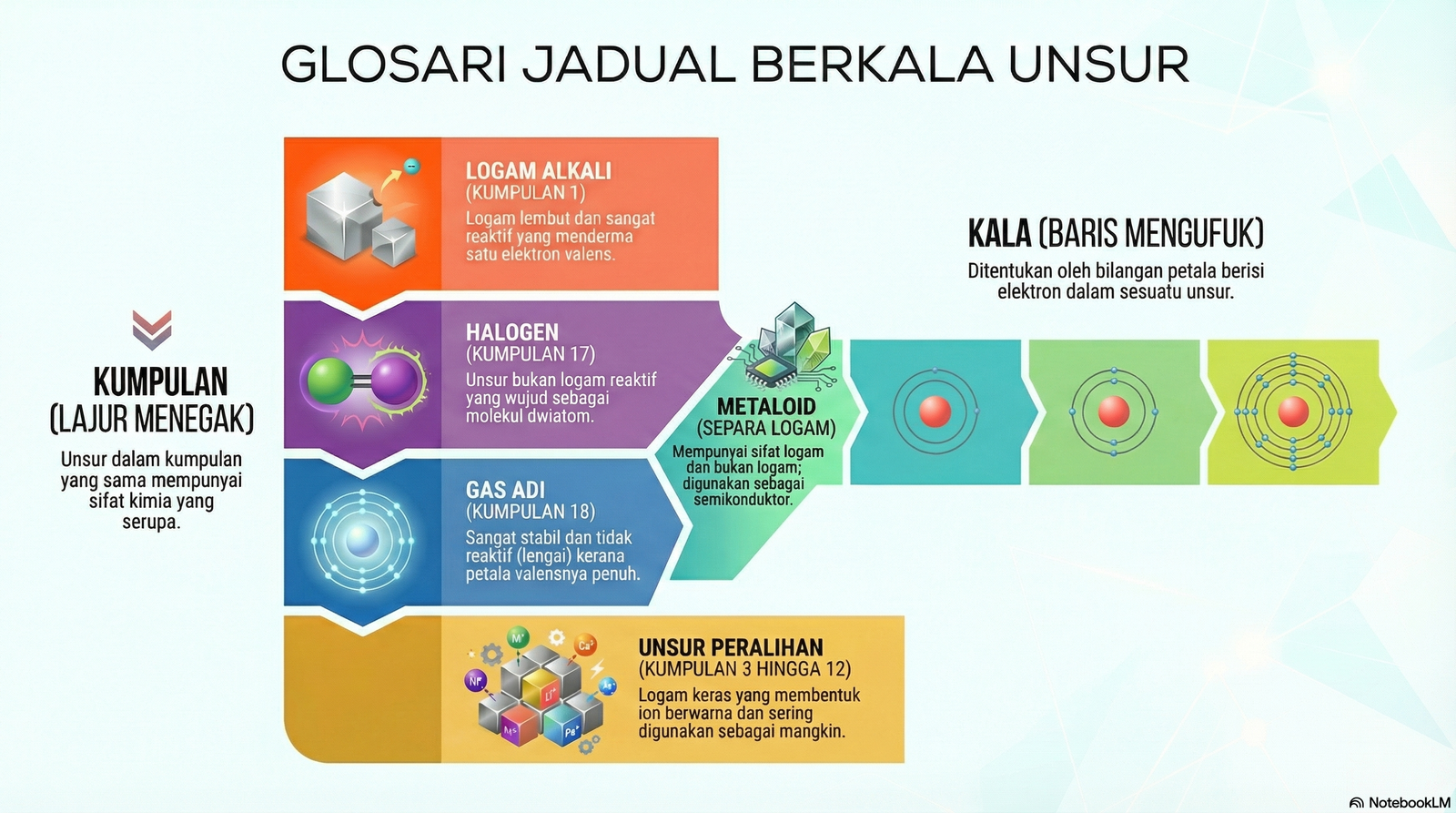
Bab 4Gas Adi
Unsur Kumpulan 18 yang tidak reaktif kerana mempunyai petala valens penuh (duplet/oktet).
Bab 4Halogen
Unsur Kumpulan 17 Jadual Berkala (klorin, bromin, iodin). Wujud sebagai molekul dwiatom.
Bab 4Hukum Oktaf
Susunan John Newlands di mana sifat unsur berulang pada setiap unsur kelapan.
Bab 4Ion Kompleks
Ion yang terbentuk oleh unsur peralihan, di mana ion logam pusat dikelilingi molekul/ion lain.
Bab 4Kala
Baris mengufuk dalam Jadual Berkala ditentukan oleh bilangan petala berisi elektron.
Bab 4Keelektronegatifan
Ukuran kecenderungan sesuatu atom untuk menarik elektron dalam ikatan kimia.
Bab 4Kumpulan
Lajur menegak dalam Jadual Berkala ditentukan oleh bilangan elektron valens.
Bab 4Logam Alkali
Unsur Kumpulan 1 yang sangat reaktif seperti Litium, Natrium, dan Kalium.
Bab 4Mangkin
Bahan yang mempercepat kadar tindak balas tanpa mengalami perubahan kimia kekal.
Bab 4Metaloid
Unsur yang mempunyai kedua-dua sifat logam dan bukan logam (cth: Silikon).
Bab 4Nombor Pengoksidaan
Nombor yang mewakili darjah kehilangan atau penerimaan elektron atom dalam sebatian.
Bab 4Oksida Amfoterik
Oksida yang boleh bertindak balas dengan asid dan juga alkali (cth: Aluminium Oksida).
Bab 4Susunan Elektron Duplet
Susunan stabil dengan 2 elektron pada petala valens (cth: Helium).
Bab 4Susunan Elektron Oktet
Susunan stabil dengan 8 elektron pada petala valens.
Bab 4Unsur Peralihan
Unsur antara Kumpulan 2 & 13. Berfungsi sebagai mangkin dan membentuk ion berwarna.
Bab 4