Nota Kimia Tingkatan 5 Bab 1: Keseimbangan Redoks
Bab 1: Keseimbangan Redoks
Nota Interaktif • Tingkatan 5 KSSM
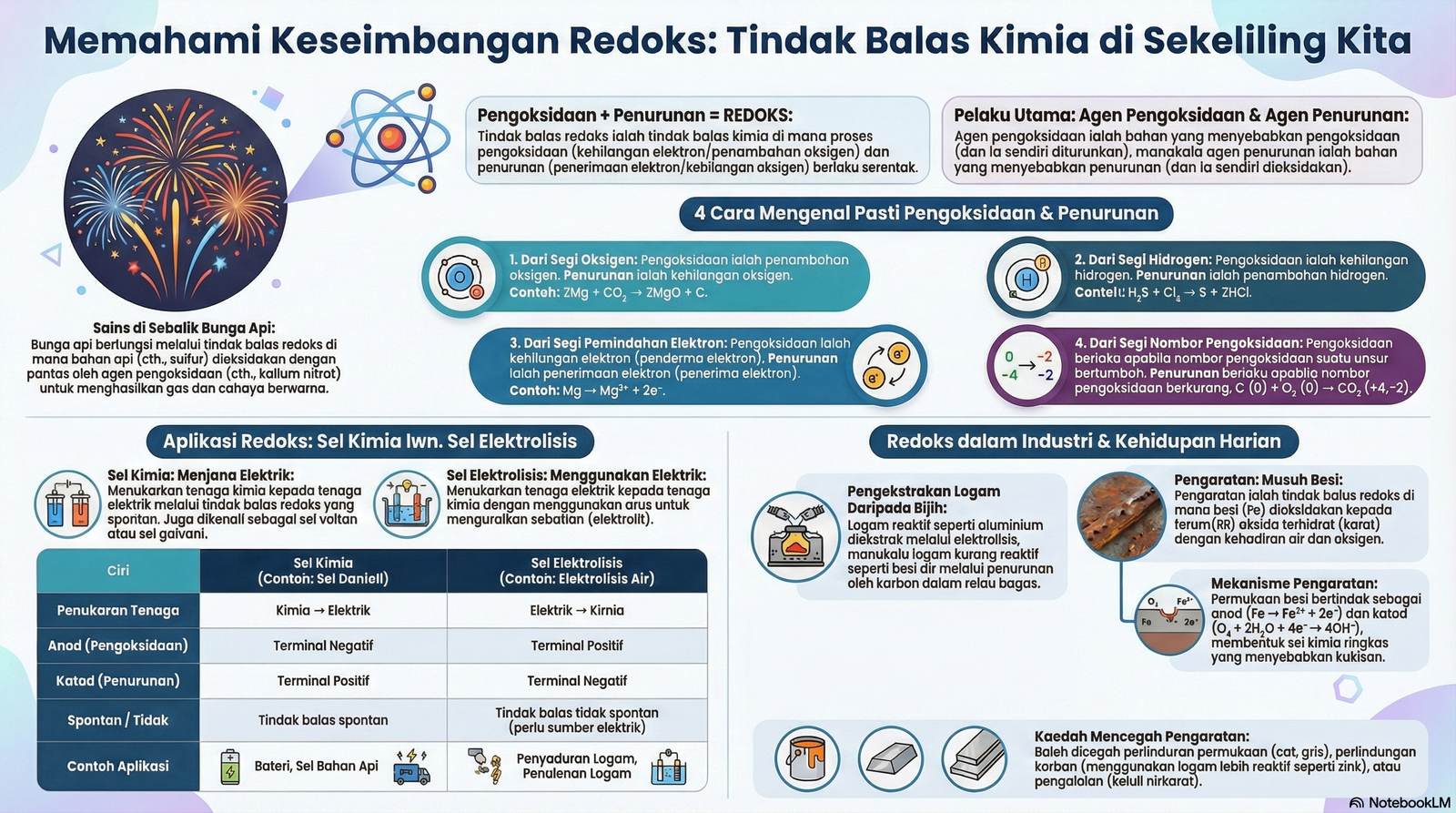
1.1 Apakah itu Tindak Balas Redoks?
Tindak balas Redoks adalah singkatan bagi proses REDuction (Penurunan) dan OXidation (Pengoksidaan) yang berlaku secara serentak dalam satu tindak balas.
🔥 Pengoksidaan (Oxidation)
- Terima Oksigen
- Hilang Hidrogen
- Derma / Hilang Elektron
- Nombor Pengoksidaan Meningkat
🧊 Penurunan (Reduction)
- Hilang Oksigen
- Terima Hidrogen
- Terima Elektron
- Nombor Pengoksidaan Menurun
Agen Pengoksidaan & Agen Penurunan
Agen Pengoksidaan: Bahan yang mengoksidakan bahan lain, tetapi ia sendiri mengalami penurunan.
Agen Penurunan: Bahan yang menurunkan bahan lain, tetapi ia sendiri mengalami pengoksidaan.
Mg (Agen Penurunan), Cu2+ (Agen Pengoksidaan)
1.2 Keupayaan Elektrod Piawai (E0)
Keupayaan elektrod piawai (E0) ialah beza keupayaan yang terhasil apabila suatu separuh sel disambungkan kepada Elektrod Hidrogen Piawai (SHE).
- Suhu piawai: 298K (25°C)
- Tekanan gas: 1 atm
- Kepekatan larutan akueus: 1.0 mol dm-3
- Nilai E0 bagi SHE ialah 0.00 V
Nilai E0 Lebih Positif (+)
Bahan lebih mudah menerima elektron dan mengalami penurunan. Ia adalah Agen Pengoksidaan yang kuat. (Cth: Fluorin, F2, E0 = +2.87V)
Nilai E0 Lebih Negatif (-)
Bahan lebih mudah melepaskan elektron dan mengalami pengoksidaan. Ia adalah Agen Penurunan yang kuat. (Cth: Litium, Li, E0 = -3.04V)
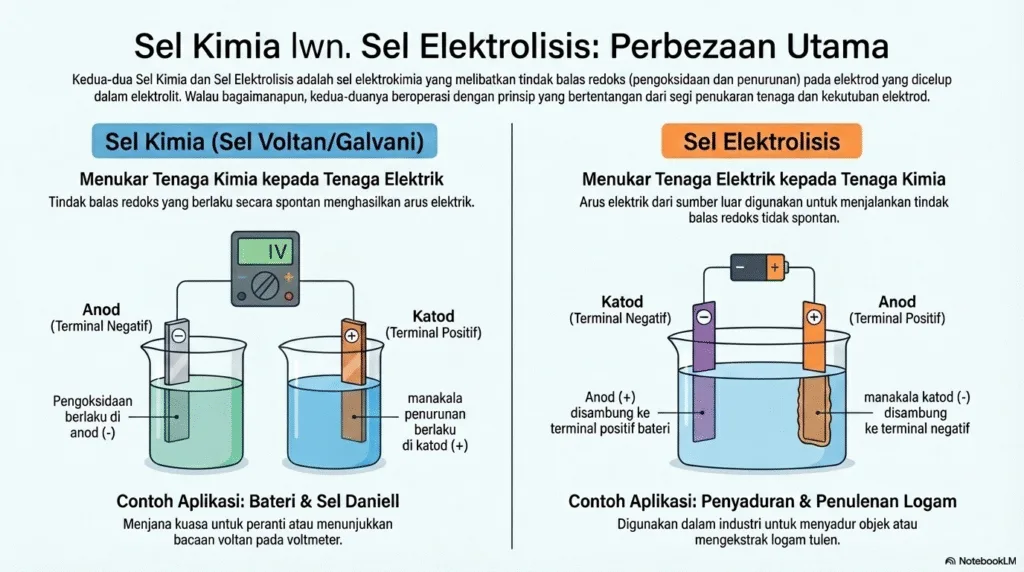
1.3 & 1.4 Sel Kimia & Sel Elektrolisis
Perbandingan antara dua jenis sel yang penting dalam siri elektrokimia.
| Ciri-ciri | Sel Kimia (Sel Volta) | Sel Elektrolisis |
|---|---|---|
| Perubahan Tenaga | Tenaga Kimia → Tenaga Elektrik | Tenaga Elektrik → Tenaga Kimia |
| Anod (Pengoksidaan) | Terminal Negatif (-) | Terminal Positif (+) |
| Katod (Penurunan) | Terminal Positif (+) | Terminal Negatif (-) |
| Aliran Elektron | Mengalir dari Anod ke Katod melalui litar luar | |
Animasi: Pergerakan Elektron dalam Sel Kimia (Sel Daniell)
Pengoksidaan (Derma e–)
Penurunan (Terima e–)
1. Kedudukan ion dalam Siri Elektrokimia (E0)
2. Kepekatan larutan (Hanya mempengaruhi Anod/Anion)
3. Jenis elektrod yang digunakan (Aktif/Karbon)
1.5 Pengekstrakan Logam daripada Bijihnya
Kaedah pengekstrakan bergantung kepada kedudukan logam dalam Siri Kereaktifan Logam.
⚡ Logam Sangat Reaktif
Kalium (K), Natrium (Na), Kalsium (Ca), Magnesium (Mg), Aluminium (Al)
Diekstrak melalui kaedah Elektrolisis leburan bijih logam. Logam-logam ini terlalu stabil untuk diturunkan oleh Karbon.
🔥 Logam Sederhana Reaktif
Zink (Zn), Besi (Fe), Timah (Sn), Plumbum (Pb)
Diekstrak melalui proses Penurunan oleh Karbon dalam relau bagas. (Karbon terletak di antara Al dan Zn dalam siri kereaktifan).
*Logam yang paling tidak reaktif seperti Emas (Au) dan Perak (Ag) wujud sebagai unsur bebas dalam kerak bumi.
1.6 Pengaratan
Pengaratan ialah kakisan logam yang khusus berlaku pada Besi (Ferum, Fe). Ia merupakan satu proses redoks semula jadi.
Syarat Berlakunya Pengaratan:
Mesti mempunyai kehadiran Air (H2O) dan Oksigen (O2).
Faktor Mempercepatkan: Kehadiran asid atau garam (seperti air laut).
| Mekanisme | Penerangan / Persamaan Separuh |
|---|---|
| Anod (-) | Besi dioksidakan menjadi ion Ferum(II). Fe → Fe2+ + 2e– |
| Katod (+) | Air dan Oksigen menerima elektron diturunkan menjadi ion Hidroksida. O2 + 2H2O + 4e– → 4OH– |
| Pembentukan Karat | Fe2+ dan OH– bergabung membentuk Ferum(II) hidroksida, kemudian dioksidakan oleh udara menjadi Ferum(III) oksida terhidrat (Karat Perang). |
🛡️ Cara Pencegahan
- Permukaan: Mengecat, menyapu minyak/gris, membalut dengan plastik.
- Pengaloian: Mengadun besi dengan karbon/kromium menjadi keluli nirkarat (Stainless steel).
- Logam Korban: Menyambungkan besi dengan logam yang lebih elektropositif (Cth: Zink, Magnesium). Logam tersebut akan terkakis, manakala besi terselamat.
Koleksi Latihan
| 1 | 2 |
| 3 | 4 |
| 5 | 6 |
GLOSARI DIGITAL REDOKS
Tindak Balas Redoks
Tindak balas kimia di mana pengoksidaan dan penurunan berlaku secara serentak.
Pengoksidaan
Proses yang melibatkan: penambahan oksigen, kehilangan hidrogen, menderma elektron, atau pertambahan nombor pengoksidaan.
Penurunan
Proses yang melibatkan: kehilangan oksigen, penambahan hidrogen, menerima elektron, atau pengurangan nombor pengoksidaan.
Elektrolisis
Proses penguraian elektrolit dalam keadaan lebur atau akueus menggunakan arus elektrik kepada unsur juzuknya.
Pengaratan
Tindak balas redoks khusus pada besi dengan oksigen dan air untuk membentuk ferum(III) oksida terhidrat (karat).
Penyesaran
Logam yang lebih elektropositif menyesarkan logam yang kurang elektropositif daripada larutan garamnya.
Agen Pengoksidaan
Bahan yang menyebabkan pengoksidaan pada bahan lain tetapi ia sendiri mengalami penurunan (menerima elektron).
Agen Penurunan
Bahan yang menyebabkan penurunan pada bahan lain tetapi ia sendiri mengalami pengoksidaan (menderma elektron).
Elektrolit
Bahan yang mengalirkan arus elektrik dalam keadaan lebur atau akueus melalui pergerakan ion bebas.
Anod
Elektrod tempat pengoksidaan berlaku. (Terminal negatif dalam sel kimia; positif dalam sel elektrolisis).
Katod
Elektrod tempat penurunan berlaku. (Terminal positif dalam sel kimia; negatif dalam sel elektrolisis).
Sel Kimia
Peranti yang menukarkan tenaga kimia kepada tenaga elektrik melalui tindak balas redoks spontan.
Sel Elektrolisis
Peranti yang menggunakan tenaga elektrik untuk menjalankan tindak balas redoks tidak spontan.
No. Pengoksidaan
Cas khayalan yang dimiliki oleh suatu unsur dalam sebatian jika pemindahan elektron berlaku sepenuhnya.
Keupayaan Elektrod ($E^0$)
Beza keupayaan yang terhasil dalam sistem keseimbangan elektrod pada keadaan piawai (25°C, 1 atm).
Siri Elektrokimia
Penyusunan logam mengikut tertib keupayaan elektrod piawai dari paling negatif ke paling positif.
CABARAN MINDA KBAT
5 MODUL
Uji kefahaman anda dengan senario dunia sebenar dan aplikasi industri elektrokimia.
Kesan Calar pada Tin Makanan
Sebuah tin keluli disadur dengan timah (Sn). Apabila tin kemik dan tercalar, mengapa pengaratan pada bahagian calar berlaku lebih cepat daripada besi biasa?
Besi (Fe) lebih elektropositif daripada Timah (Sn). Fe bertindak sebagai anod manakala Sn sebagai katod.
Kelembapan bertindak sebagai elektrolit, membentuk sel kimia ringkas di mana Fe dioksidakan dengan pantas.
Penurunan: $O_2(g) + 2H_2O(ce) + 4e^- \rightarrow 4OH^-(ak)$
Kesimpulan: Timah mewujudkan sel elektrokimia di mana besi menjadi anod korban, mempercepatkan kakisan.
Pengekstrakan Aluminium
Mengapa kriolit ditambah ke dalam leburan $Al_2O_3$ dan mengapa anod karbon perlu diganti secara berkala dalam proses ini?
Peranan Kriolit ($Na_3AlF_6$):
Merendahkan takat lebur $Al_2O_3$ dari ~2000°C ke suhu yang lebih rendah untuk menjimatkan kos tenaga.
Isu Anod Karbon:
Oksigen yang terhasil di anod bertindak balas dengan karbon pada suhu tinggi untuk membentuk gas $CO_2$. Ini menyebabkan anod terhakis.
Analisis Sel Mg | Cu
Diberi $E^0$ Mg = -2.38 V dan $E^0$ Cu = +0.34 V. Tentukan notasi sel dan hitung voltan sel ($E^0$ sel).
Anod (-) / Pengoksidaan
Magnesium (Mg)
Katod (+) / Penurunan
Kuprum (Cu)
Notasi Sel:
Pengiraan:
$E^0_{sel} = E^0_{katod} - E^0_{anod}$
$E^0_{sel} = (+0.34) - (-2.38) = +2.72 V$
Redoks dalam Bunga Api
Kenal pasti agen pengoksidaan dan agen penurunan dalam campuran bunga api ($KNO_3$, Arang, Sulfur).
- Agen Pengoksidaan: $KNO_3$ (Membekalkan oksigen, ia sendiri mengalami penurunan).
- Agen Penurunan: Karbon & Sulfur (Bahan api yang dioksidakan untuk menghasilkan gas dan tenaga).
Perbandingan Elektrod Lengai vs Aktif
Bandingkan pemerhatian di anod bagi elektrolisis $CuSO_4$ menggunakan elektrod Karbon (I) dan elektrod Kuprum (II).
Set I: Karbon (Lengai)
Pemerhatian: Gelembung gas oksigen terbebas.
Ion $OH^-$ dipilih untuk dinyahcas berdasarkan nilai $E^0$ yang lebih negatif.
Set II: Kuprum (Aktif)
Pemerhatian: Anod semakin nipis (melarut).
Faktor jenis elektrod mengatasi nilai $E^0$. Atom Cu sendiri dioksidakan menjadi ion $Cu^{2+}$.
