Nota Sains Tambahan Tingkatan 5 Bab 4: Tenaga Dan Perubahan Kimia
Nota Interaktif Sains
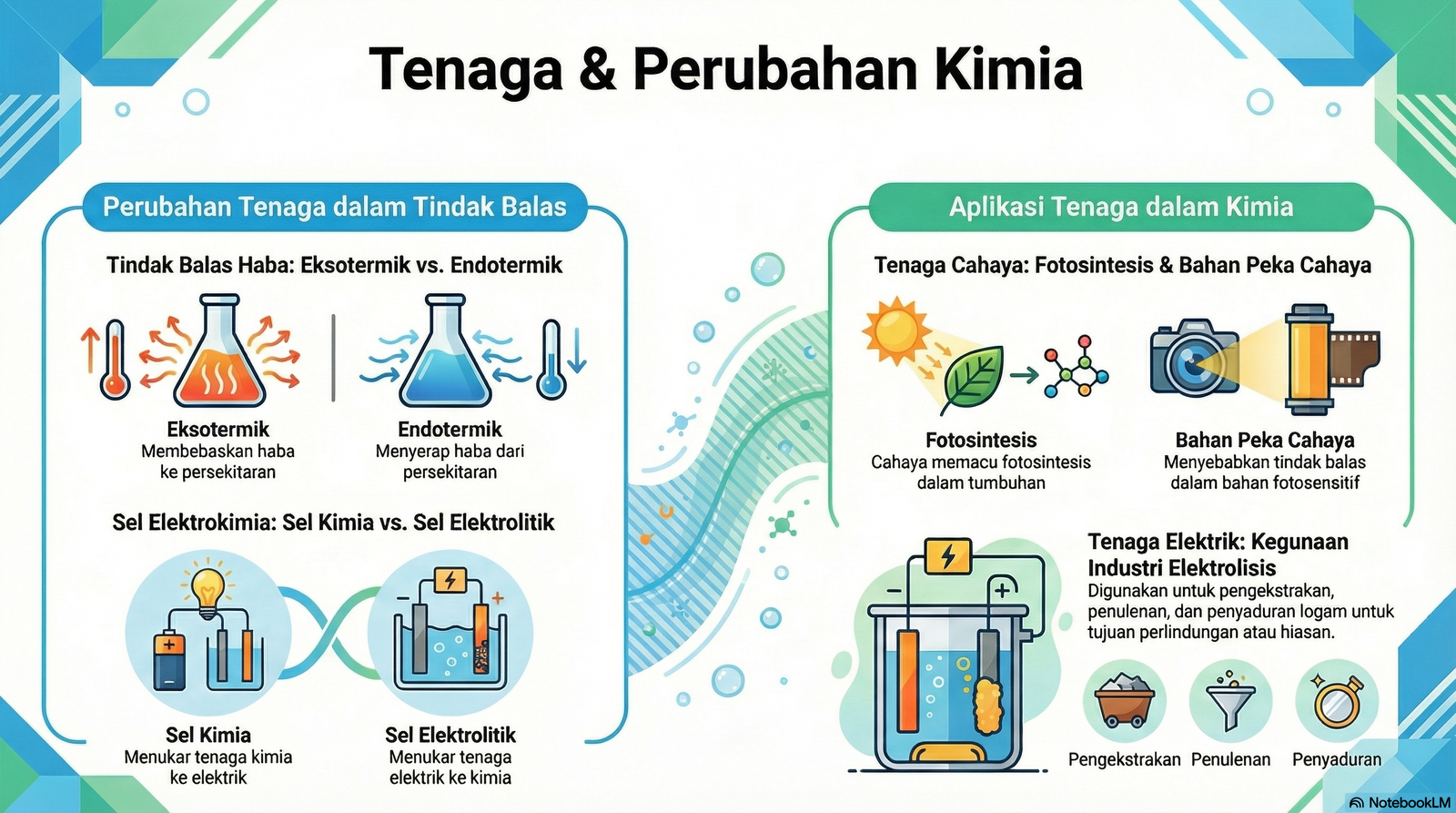
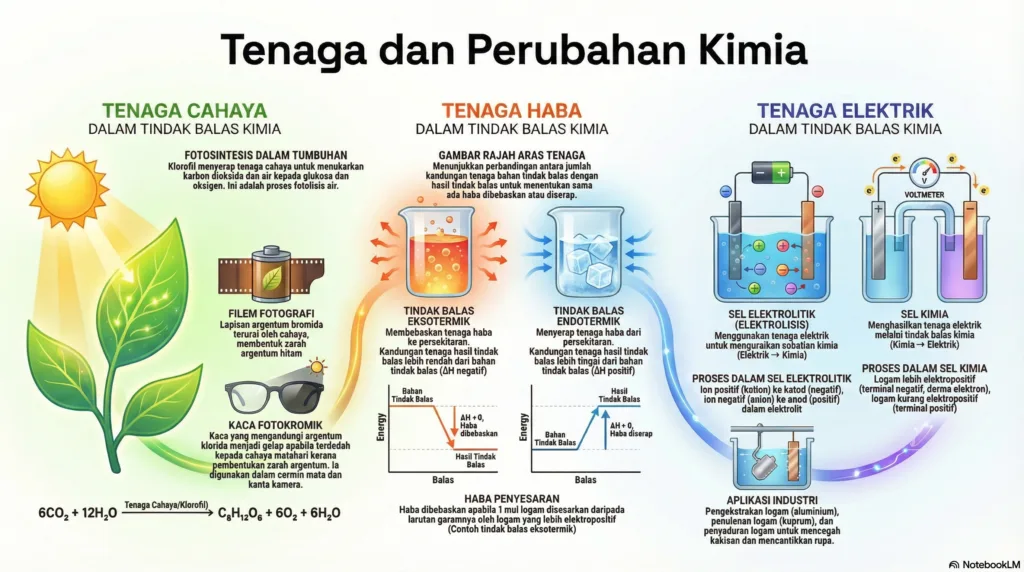
Bab 4: Tenaga dan Perubahan Kimia
Tindak balas kimia yang memerlukan tenaga cahaya dipanggil tindak balas fotokimia (bahan fotosensitif). Cahaya memecahkan atau mengubah struktur kimia bahan tersebut.
Animasi: Kanta Fotokromik
UV bertindak ke atas Argentum Klorida memgelapkan kanta.
Aplikasi Harian
-
Filem Fotografi: Disaluti lapisan Argentum Bromida (AgBr). Apabila terdedah kepada cahaya, ia terurai membentuk zarah argentum hitam dan gas bromin.
2AgBr → 2Ag + Br2 - Kanta Fotokromik: Cermin mata bertukar menjadi gelap di bawah cahaya matahari kerana kehadiran hablur Argentum Klorida (AgCl).
- Ubat-ubatan: Disimpan dalam botol kaca gelap (legap) untuk mengelakkan ubat rosak/terurai akibat pendedahan tenaga cahaya.
Tindak balas kimia sentiasa disertai dengan perubahan tenaga haba, dibahagikan kepada dua jenis utama iaitu Eksotermik dan Endotermik.
Eksotermik
- Membebaskan haba ke persekitaran.
- Suhu persekitaran meningkat (terasa panas).
- Contoh: Pembakaran bahan api, Peneutralan, Pengekstrakan logam.
Endotermik
- Menyerap haba dari persekitaran.
- Suhu persekitaran menurun (terasa sejuk).
- Contoh: Penguraian terma, Melarutkan garam ammonium.
Animasi: Perubahan Suhu
Terdapat hubungan dua hala yang rapat antara tenaga elektrik dan bahan kimia yang melibatkan pemindahan elektron pada elektrod (Anod & Katod).
Animasi: Penyaduran Kunci (Sel Elektrolisis)
Jenis Sel
-
Sel Elektrolitik (Elektrolisis):
Menukarkan Tenaga Elektrik → Tenaga Kimia.
Aplikasi Industri:- Penyaduran: Menyalut logam murah dengan logam berharga. Objek di Katod, Logam penyadur di Anod.
- Penulenan: Memurnikan logam tak tulen (Anod) menjadi tulen (Katod).
-
Sel Kimia (Sel Volta / Galvani):
Menukarkan Tenaga Kimia → Tenaga Elektrik.
Terdiri dari 2 logam berbeza yang dicelup ke dalam elektrolit (Cth: Bateri atau sel kering).
GLOSARI SAINS DIGITAL
Eksotermik
Tindak balas kimia yang membebaskan tenaga haba ke persekitaran, menyebabkan suhu meningkat.
Endotermik
Tindak balas kimia yang menyerap tenaga haba dari persekitaran, menyebabkan suhu menurun.
Haba Penyesaran
Haba dibebaskan apabila 1 mol logam disesarkan daripada larutan garamnya oleh logam lebih elektropositif.
Elektrolisis
Proses penguraian sebatian (elektrolit) dalam keadaan lebur/akueus oleh pengaliran arus elektrik.
Sel Elektrolitik
Radas yang menukarkan tenaga elektrik kepada tenaga kimia melalui elektrod dan elektrolit.
Sel Kimia
Sel yang menghasilkan tenaga elektrik secara spontan daripada tindak balas kimia di dalamnya.
Penyaduran
Menyalut permukaan logam dengan lapisan nipis logam lain melalui elektrolisis untuk perlindungan/hiasan.
Penulenan
Proses mengasingkan bendasing daripada logam tidak tulen untuk mendapatkan hasil yang lebih bersih.
Pengekstrakan
Proses mendapatkan logam daripada bijih mentah melalui kaedah kimia atau elektrikal.
Fotokromik
Kaca mengandungi argentum halida yang menjadi gelap secara automatik apabila terkena cahaya matahari.
Fotolisis Air
Pemecahan molekul air kepada ion hidrogen dan oksigen menggunakan tenaga cahaya (dalam fotosintesis).
Fotosensitif
Bahan kimia yang peka terhadap cahaya dan mudah terurai apabila terdedah kepada sinaran cahaya.
HOTS / KBAT
ZON PEMIKIRAN KRITIS
Analisis mendalam mengenai aplikasi tenaga haba, elektrik, dan cahaya dalam sistem kimia.
Mengapakah botol gelap diperlukan untuk penyimpanan Argentum Bromida?
Botol Gelap
Menghalang cahaya daripada memulakan tindak balas fotosensitif. Argentum bromida dikekalkan dalam bentuk sebatian tulen.
Kesan Cahaya
Mencetuskan penguraian:
2AgBr $\rightarrow$ 2Ag + $Br_2$
Menghasilkan argentum hitam dan gas bromin.
Analisis Perbezaan Sel Kimia Ringkas vs Sel Elektrolitik (Penulenan)
| Ciri Perbandingan | Sel Kimia (Mg-Cu) | Sel Elektrolitik (Penulenan) |
|---|---|---|
| Perubahan Tenaga | Kimia $\rightarrow$ Elektrik | Elektrik $\rightarrow$ Kimia |
| Terminal Negatif | Magnesium (Anod) | Katod (Cu Tulen) |
| Aliran Elektron | Mg $\rightarrow$ Cu (Litar Luar) | Anod $\rightarrow$ Bateri $\rightarrow$ Katod |
| Hasil di Katod | Enapan Kuprum (Tebal) | Enapan Kuprum Tulen (Tebal) |
Reka bentuk susunan radas penyaduran sudu besi dengan kromium.
Terminal Negatif (Katod)
Sudu besi disambungkan di sini untuk menarik ion $Cr^{3+}$.
Terminal Positif (Anod)
Logam kromium tulen digunakan untuk membekalkan ion ke dalam larutan.
Elektrolit Khusus
Gunakan larutan Kromium(III) Sulfat untuk memastikan aliran ion yang betul.
Bandingkan Fotosintesis dengan Pembakaran Magnesium.
Fotosintesis
Proses Endotermik. Menyerap tenaga cahaya untuk membentuk glukosa. Aras tenaga hasil > Aras tenaga bahan.
Pembakaran Mg
Proses Eksotermik. Membebaskan haba ke persekitaran. $\Delta H = -1204$ kJ $mol^{-1}$.
Mengapa pengekstrakan aluminium sangat intensif tenaga?
-
1
Takat Lebur Ekstrim: Aluminium oksida memerlukan tenaga haba yang sangat besar untuk melebur (lebih $2000^\circ$C).
-
2
Ikatan Kimia Stabil: Ikatan dalam $Al_2O_3$ sangat kuat, memerlukan arus elektrik yang tinggi untuk pemecahan elektrolitik.
-
3
Kitar Semula (9% Tenaga): Hanya melibatkan peleburan semula logam, bukan pemecahan ikatan kimia asal.
